欢迎您注册蒲公英
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
注:收藏上面「蒲公英商城」,下单省5元 撰稿|石决明 来自|蒲公英Ouryao 引子:一篇旧文(J. Agalloco, “Kill the Bioburden, Not the Biological Indicator," BioPharm International 30 (4) 2017.)翻译概括并加入评论如下,旨在让你听到不同的声音。 一、核心认知:灭菌目标与常见误区灭菌工艺的核心目标是保障患者临床使用安全,核心任务是将进入人体、突破皮肤及肠道等常规防护屏障的产品内外微生物(即生物负载),灭杀至非无菌单元概率(PNSU)10⁻⁶的行业通用安全标准。

PNSU公式计算,明确计算需采用生物负载的实际菌量、微生物抗性指标(D值)及121℃等效致死时间(F₀值),而非行业内普遍存在的“误用生物指示剂相关数据”的误区。 例如:估计PNSU在100°C下3分钟过程,起始单位为100 CFU,估计D100为0.0003分钟。 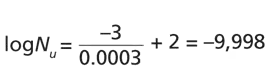 可以立即看出,这种极短且低温的灭菌过程提供了压倒性的安全性,几乎是最低预期的1万倍。生物负荷在这些条件下的湿热耐热性极低,基本没有生存机会。即使过程在100°C下持续3分钟,而非更常见的超过121°C的过程,这一点依然成立。 用传统的生物指示剂——Geobacillus stearothermophilus,无法确定这一低温过程的致死性,其抗性极强,假设过程对其种群无实质影响。 需明确的是,生物指示剂仅用于灭菌工艺的初始验证与定期验证,验证所用材料均不投入临床使用;若盲目以灭杀高抗性、高菌量的生物指示剂为目标设定灭菌参数,会无端损害被灭菌产品,本质上偏离了灭菌工艺“灭杀生物负载、保障患者安全”的核心初衷。 二、关键步骤:基于生物负载的灭菌工艺开发基于生物负载的灭菌工艺开发与验证,需严格遵循四步核心流程,确保工艺科学可行、安全可控: 一、是确定生物负载模型,可通过对灭菌前材料的针对性实验、查阅灭菌领域现有文献,或对预期生物负载作出合理假设,精准获取其实际菌量与抗性数据。二、是将生物负载的菌量、抗性等数据代入修正后的PNSU计算公式,精准核算工艺最低保压时间,确保灭菌效果达到预设安全标准。三、是选择与工艺参数适配的生物指示剂,以“部分灭杀”为核心验证标准,优先选用巨大芽孢杆菌、奥勒冈芽孢杆菌等嗜温芽孢菌,保障验证结果的说服力。四、是结合物理检测与微生物挑战试验,全面验证灭菌工艺实际达到规定致死率,确保工艺稳定性。整个过程中可合理采用最不利条件假设(如假定生物负载菌量更高、抗性更强、提高最低PNSU要求等)提升工艺可信度,但需避免过度叠加假设,防止工艺过于严苛而损害产品质量属性。三、核心原则:平衡安全与合理灭菌灭菌工艺验证的核心原则,是平衡两大相互矛盾的关键点——提升工艺无菌安全性与避免过度灭菌对产品造成损害,核心导向是围绕生物负载开展全流程工作,将生物指示剂准确定位为工艺验证的辅助工具,而非工艺参数设定的依据。 核心原因在于:生物负载贯穿产品生产全过程,是无菌产品药品生产质量管理规范(GMP)体系的关键控制对象,企业需采取针对性措施将其管控至安全水平;而生物指示剂仅用于工艺验证,且验证用材料从未用于患者临床。盲目延长保压时间、提高灭菌温度以实现生物指示剂完全灭杀,既无实际临床意义,还会对被灭菌产品造成不可逆损伤。 生物指示剂的正确用途,是检测灭菌负载内是否达到规定灭菌条件,进而保障工艺无菌安全性。此外,生物指示剂的抗性若发生波动,还会给灭菌工艺的定期再验证工作带来诸多困扰。综上,灭菌与无菌保证工作的唯一核心目标,始终是将生物负载灭杀至安全水平,确保灭菌工艺稳定、高效地产出合格产品,兼顾安全性与产品质量。 四、石决明评论本文标题具有明确的指向性,清晰凸显了“灭菌需聚焦生物负载”的核心观点,但也存在一定的误导性,易让人误解“生物指示剂在灭菌工艺中无需重视”。事实上,灭菌工艺的开发与验证固然需以生物负载为核心,但生物指示剂的不当使用,部分原因源于选用了通用型生物指示剂,而非生物指示剂本身无用。针对特殊灭菌工艺,生物指示剂可进行定制化选择,以此更好地适配工艺参数,实现精准验证。 此外,实际生产或者检验中诸多场景采用过度灭菌程序。此类情况下,选用通用型生物指示剂即可满足验证需求。
|  |手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033
|手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033