欢迎您注册蒲公英
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
Speaker : Chen Zhen, Ph.D
Company: Center for Drug Evaluation, CFDA
声明 中国通用名药发展研究报告 —— 市场准入制度研究(2012年) 由“通用名药物品种产业技术创新战略联盟”撰写发布
联盟的组成 CFDA药品审评中心、军事医学科学院毒物药物研究所发起,国家科技部批准成立于2009年8月。
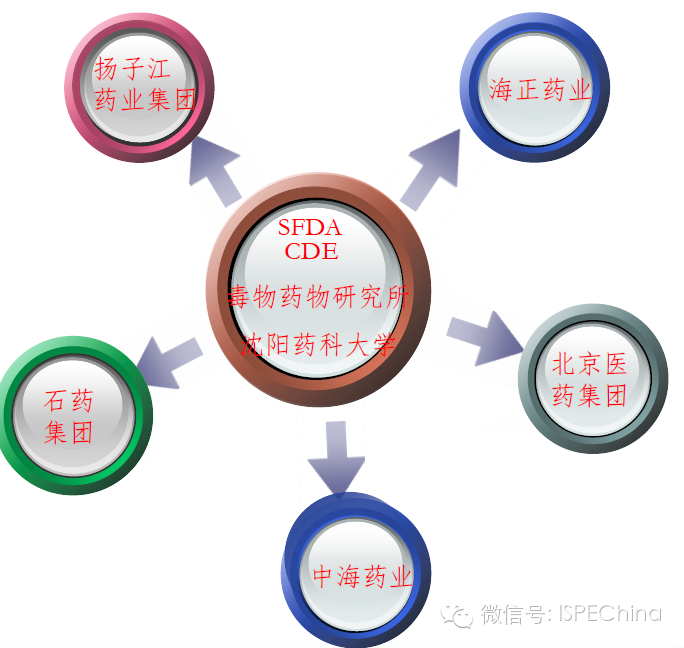
联盟的机制 国家卫生部(SFDA)、国家科技部、国家工信部 MOH (CFDA), MOST, MIIT 以国家重大需求、临床重大需求为导向,顶层设计 国家药品审评中心 建立科学的通用名药评价体系,完善相关技术指南 科研院所和大学 提供研发技术支持和政策研究支持 全国特色制药企业 完成产业化研究,整合生产能力
主要内容 我国通用名药发展的机遇 通用名药注册审评中凸显出的问题 对我国通用名药市场准入制度的分析 完善我国通用名药市场准入制度的建议
我国通用名药发展的机遇
1,我国医药产业的特点
2,我国通用名药的刚性需求增长 人均GDP超过3000美元 老龄化和城镇化加速 医保体系的建立和健全,合理资源获得最多的健康服务
作为发展中国家,通用名药是我国公共卫生政策的重要支撑
全球通用名药市场快速增长
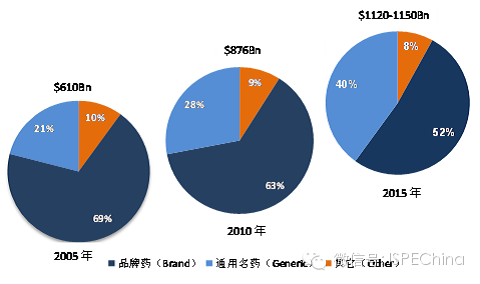
通用名药市场金额发展趋势图(2005-2015)
数据来源:The Global Use of Medicines: Outlook to 2015 by IMS Market Prognosis, 2011-9
我国成为通用名药国际竞争的重要市场
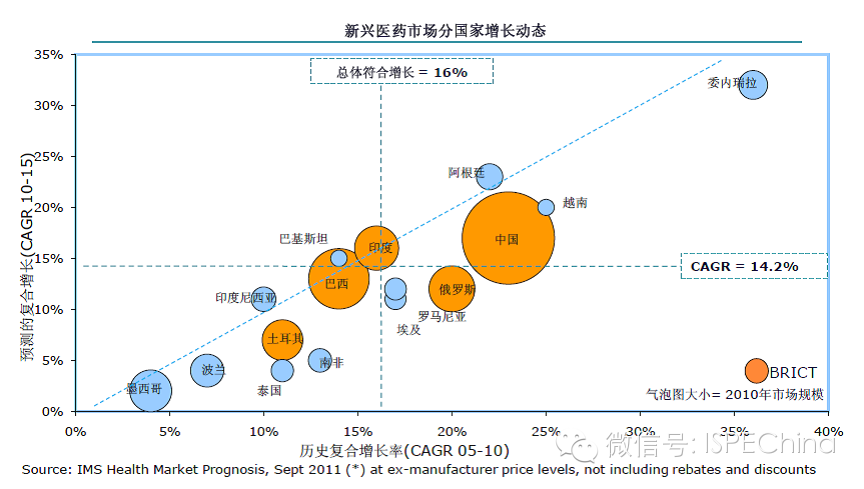
在新兴医药市场中,中国的市场规模最大,增速最快
3,大量原研药专利到期
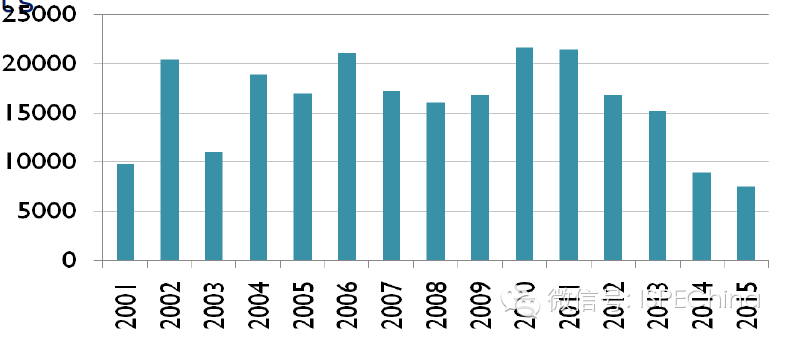 2001~2015年全球专利过期药品的市场价值
普华永道研究报告: 到2015年国际前十大制药公司共有545亿美元销售额的原研药专利过期,全球更是高达820亿美元。
通用名药注册审评中凸显出的问题
• 通用名药重复开发严重,“过剩”和“短缺”并存
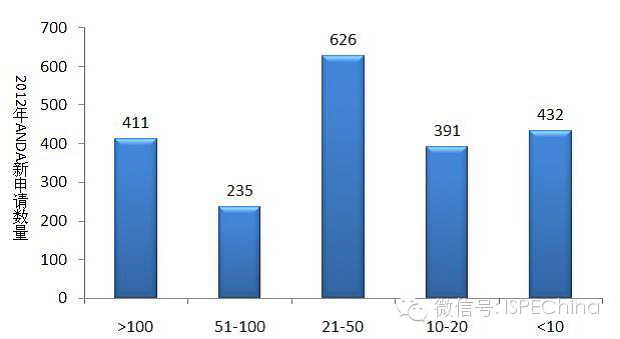
2012年新申报的ANDA申请共2095个。其中已有批准文号20个以上的药品,仍有1272个申请,占全年ANDA申报量的60.7%,已有批准文号10个以内的仅占20.6%。
• 注册审评审批耗时过长,延缓了通用名药的上市进程 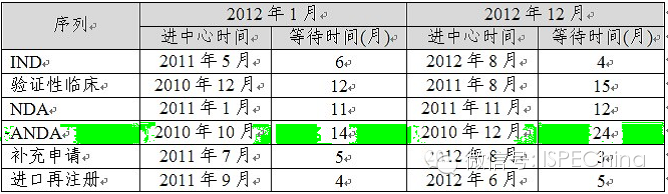
无形中延长了原研药的专利期 损害了通用名药申请人的正当利益 使公众不能及时获得质优价廉的通用名药
• 基于商业规模的研发能力不足,难以迅速形成生产力保证市场供给
CFDA于2011年8月1日发文: 截止2012年2月底,仅1/3的企业能够“举手发言”,意味着2/3的企业尚不具备工业化生产能力就提出了注册申请
原因分析
• 通用名药市场准入制度不完善 未建立上市许可人制度 未建立原辅料的DMF制度 未建立处方药和非处方药分类管理制度 未建立专利链接制度 缺乏对国家重大需求、临床亟需品种的优先审评机制 对我国通用名药市场准入制度的分析
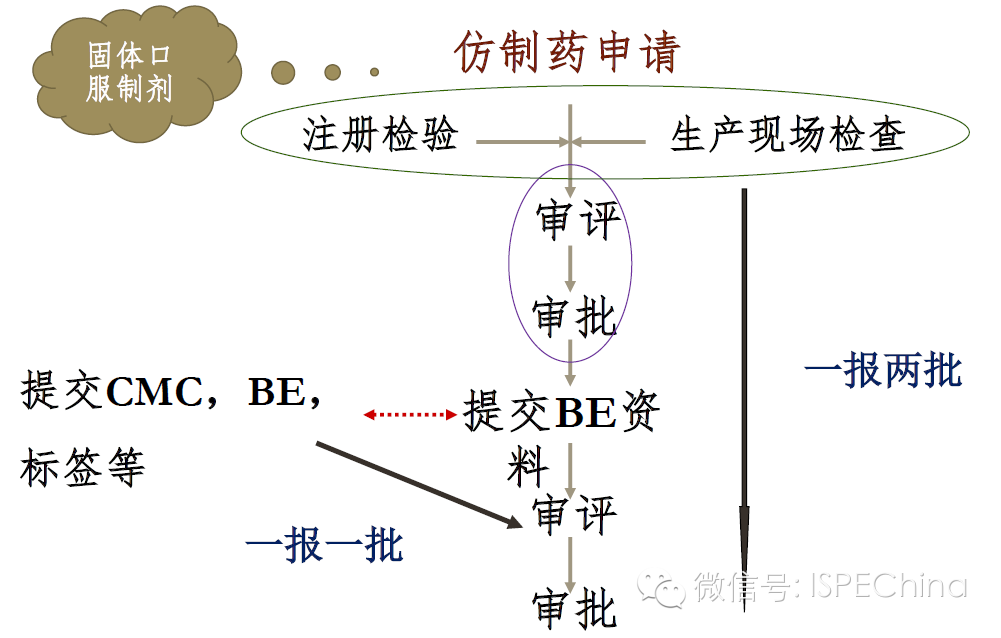 通用名药的“一报两批”制度 通用名药的“一报两批”制度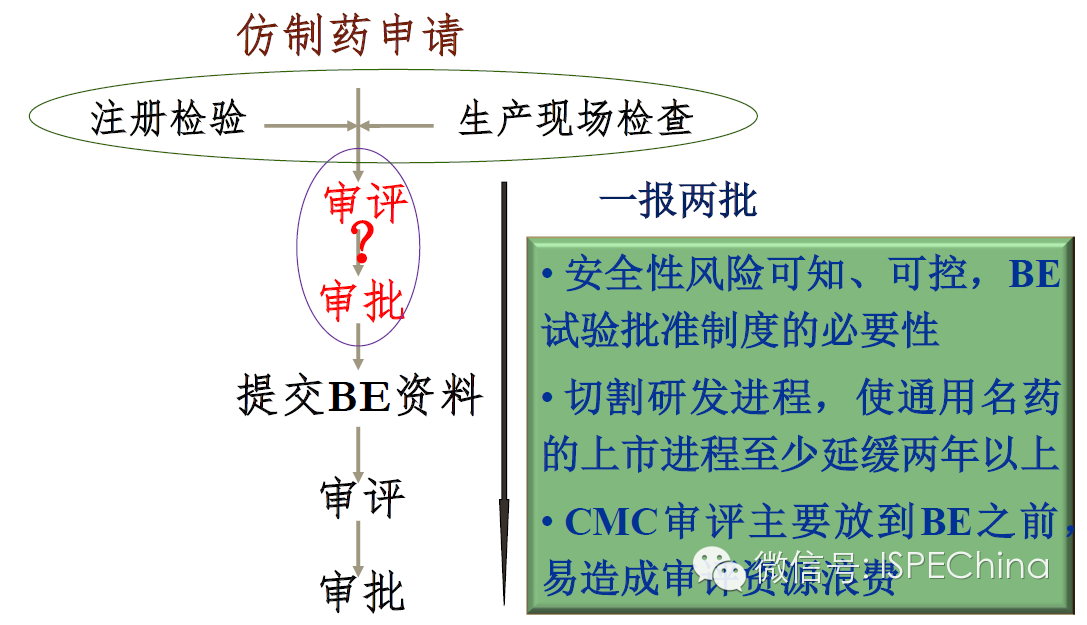 生产现场检查的时间点 生产现场检查的时间点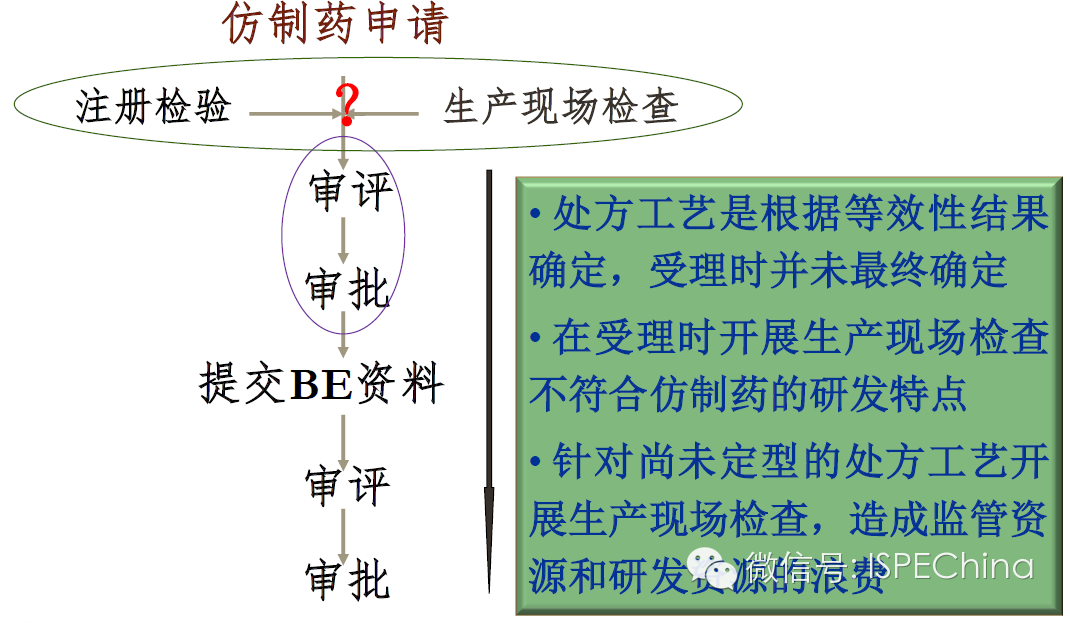 BE试验的参比制剂目录 BE试验的参比制剂目录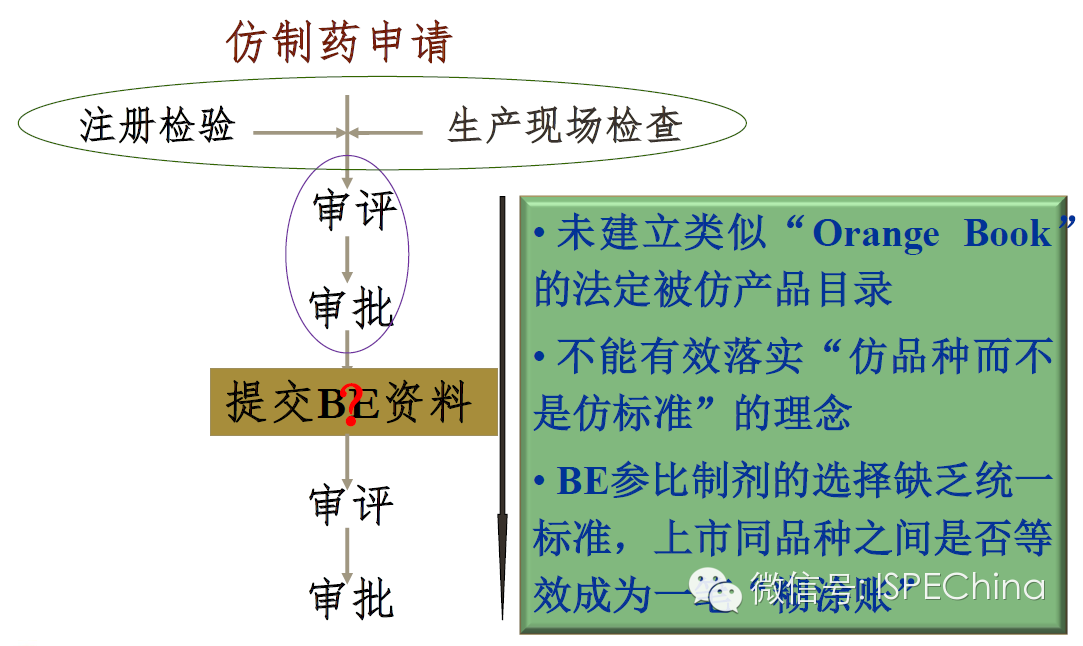 专利链接制度和专利挑战制度 专利链接制度和专利挑战制度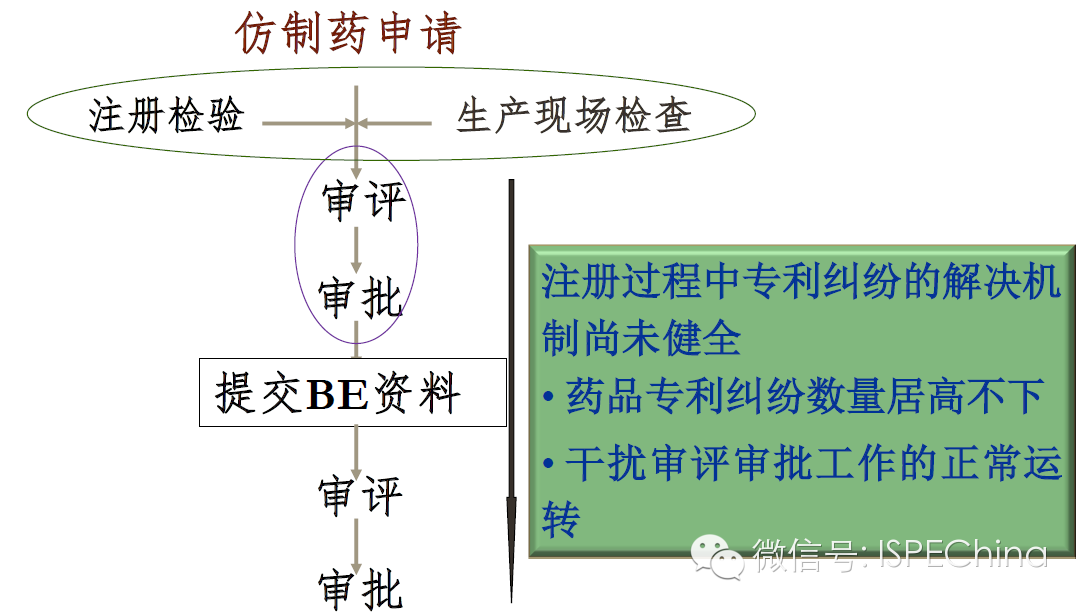 完善我国通用名药市场准入制度的建议 完善我国通用名药市场准入制度的建议- 尽快研究解决我国通用名药市场准入制度的核心问题
- 制订我国通用名药的产业发展规划推动产业结构调整
- 完善国家配套的相关政策措施促进我国通用名药的发展
关于完善我国通用名药市场准入制度的具体建议- 尽快建立通用名药的“一报一批”制度,生产现场检查后置到技术审评过程中:仿制药流程再造
- 进一步调整审评策略:资料链接现场
- 逐步建立法定的被仿产品目录
- 探索构建临床亟需仿制药的优先审评审批制度
- 进一步推动药品注册技术要求与国际接轨
- 尽快全面实施药品注册申请的CTD格式申报
• 我国医药产业“多,小,散,低”的产业格局没有根本性改变,研发投入不足,创新能力不强
• 审评能力严重不足,不能满足我国通用名药快速发展的要求,体现在审评人员的数量少、专业不全、能力不足
• 相关政策对通用名药研发投入和发展的激励尚显不足 国家针对通用名药的产业发展规划需要进一步明确 上市后招标、定价、医保、报销等机制需要不断完善
|  |手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033
|手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033