欢迎您注册蒲公英
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
细胞死亡是维持生物发育和内部环境稳态的生理过程。靶向细胞死亡相关通路杀死癌细胞是癌症治疗的一大方向。近期,有研究团队发现和鉴定了一种 全新的细胞死亡类型——双硫死亡 (Disulfidptosis),为癌治疗开辟了新的可能性。
溶质载体家族成员 SLC7A11(Solute Carrier Family 7 Member 11,又名 xCT)是溶质转运第 7 家族的第 11 个成员,属于胱氨酸/谷氨酸逆向转运蛋白,主要参与氨基酸在质膜上的转运。这也是癌细胞赖以存活的重要通路。
2020年,德克萨斯大学 MD 安德森癌症中心的甘波谊教授研究组发现,SLC7A11 介导的,将摄入的胱氨酸还原为半胱氨酸的过程,高度依赖于 葡萄糖-戊糖磷酸途径 生成的 还原型烟酰胺腺嘌呤二核苷酸磷酸 (NADPH) [1]。
因此,在葡萄糖匮乏时,SLC7A11 高表达细胞内的 NADPH 会迅速耗竭,胱氨酸等二硫化物异常积累,从而诱发 二硫化物应激 (disulfide stress) 和细胞快速死亡。
然而,这是何种细胞死亡类型以及二硫化物应激触发细胞死亡的机制仍然未知。
重大发现2023 年 2 月 6 日,MD 安德森癌症中心的甘波谊教授和陈俊杰教授团队(刘晓光博士和聂立通博士为共同第一作者)联合在 Nature cell biology 发表了后续研究 Actin cytoskeleton vulnerability to disulfide stress mediates disulfidptosis ,揭示了这种二硫化物应激诱导的细胞死亡的机制,并将这种全新的细胞死亡类型命名为 双硫死亡 (Disulfidptosis) 。

研究发现,葡萄糖匮乏诱导的 SLC7A11 高表达癌细胞死亡不属于任何一种已知的细胞死亡类型。
这种新的细胞死亡类型既不能被一般用于抑制细胞死亡的药物抑制,也不能通过敲除铁死亡/细胞凋亡关键基因来阻止。而 硫醇氧化剂(如二酰胺和马来酸二乙酯)则可以显著增强这种细胞死亡,因此该细胞类型方式被命名为双硫死亡。
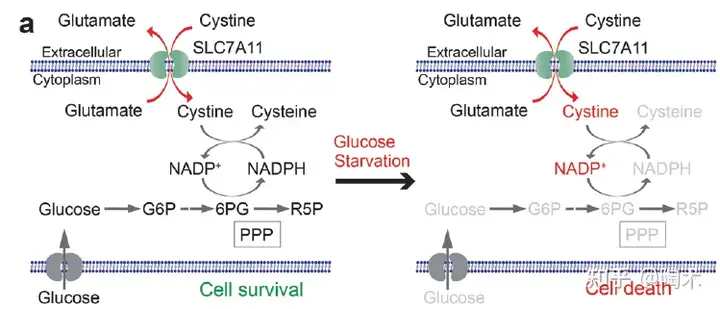
▲胱氨酸代谢和葡萄糖衍生磷酸戊糖途径(PPP)代谢途径
与其它细胞死亡机制不同,双硫死亡与 肌动蛋白细胞骨架 (actin cytoskeleton) 有关。
肌动蛋白细胞骨架是一种对维持细胞形状和存活至关重要的细胞结构,由肌动蛋白丝组成,肌动蛋白丝赋予细胞整体形状和结构。
生物正交化学蛋白组学实验表明,在 SLC7A11high UMRC6 肾癌细胞中,葡萄糖匮乏时二硫键增加最显著的蛋白主要集中在 肌动蛋白细胞骨架 和 细胞粘附 相关的生物过程或途径。
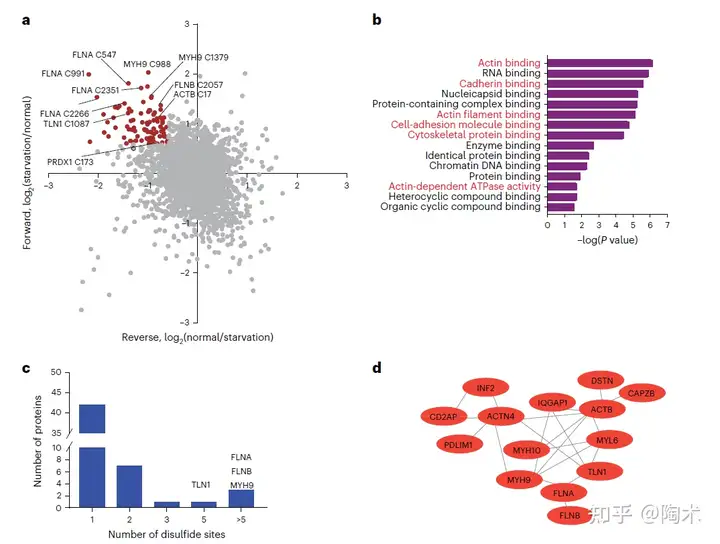
▲葡萄糖缺乏SLC7A11high细胞的蛋白质组学分析
在肌动蛋白细胞骨架蛋白的双硫死亡过程中,荧光染色显示葡萄糖匮乏会引起显著的 肌动蛋白丝聚集和细胞收缩。提示了肌动蛋白丝在双硫死亡中可能具有重要作用。而位于双硫死亡所需基因 (即该基因的敲除会抑制双硫死亡) 列表第四位的NCKAP1,与促进肌动蛋白聚合和片状伪足 (lamellipodia) 形成有关,其敲除确实明显减缓了双硫死亡。 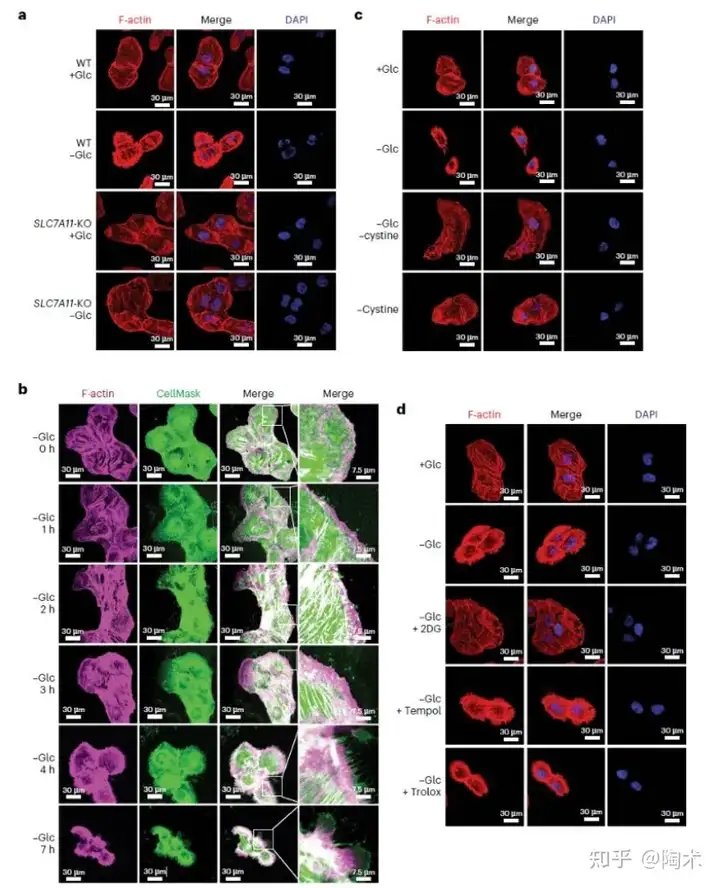
▲双硫死亡过程中肌动蛋白丝收缩
进一步研究表明, NCKAP1 缺失并不影响 SLC7A11 和 SLC3A2 蛋白水平、胱氨酸摄入或 NADP+/NADPH 比率(即 NADPH 消耗),但会减弱葡萄糖耗竭诱导的二硫键形成、 肌动蛋白骨架收缩以及与细胞质膜的脱离。
而过表达 Rac1 激活 NCKAP1 与其他亚基组成 WAVE 调节复合物 (WRC),会促进细胞片状伪足形成和双硫死亡。表明 Rac1-WRC 介导的片状伪足形成促进了双硫死亡 ,这可能是因为片状伪足中的肌动蛋白网络分支为二硫化物应激提供了关键靶点。
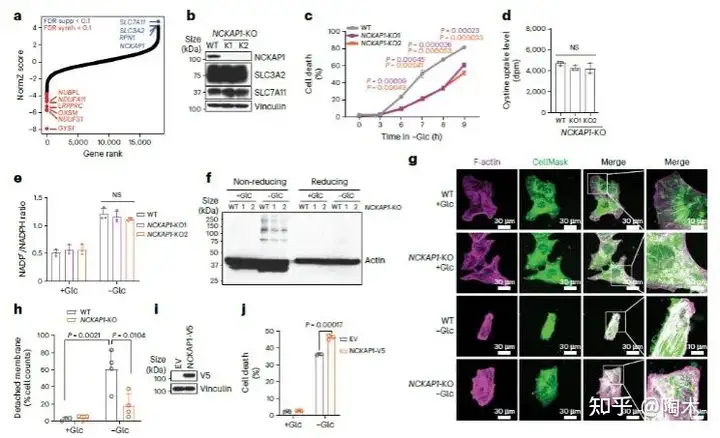
▲WRC和Rac调节双硫死亡
研究还发现,葡萄糖转运蛋白 GLUT1 抑制剂 BAY-876 和 GLUT1/3 抑制剂 KL-11743 能够有效抑制细胞的葡萄糖摄入,进而在 SLC7A11 高表达癌细胞中造成NADPH 消耗、肌动蛋白细胞骨架交联和双硫死亡。小鼠体内实验也证实了 GLUT 抑制剂能够显著抑制 SLC7A11 高表达的肿瘤生长并诱导肌动蛋白细胞骨架蛋白的异常二硫键交联。
综上,本研究发现了一种全新的细胞死亡机制,在葡萄糖匮乏的 SLC7A11high UMRC6 细胞中,大量积累的二硫键导致肌动蛋白细胞骨架蛋白之间的异常二硫键交联和细胞骨架收缩,干扰其组织并最终导致肌动蛋白网络崩溃和细胞死亡。
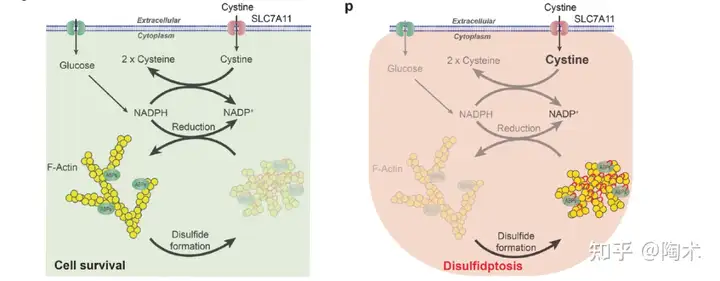
▲葡萄糖和 SLC7A11 如何协调调节肌动蛋白细胞骨架二硫化物稳态的工作模型
这一发现有望治疗那些逃避其它疗法并对细胞凋亡有抵抗力的癌症,其中 GLUT 抑制剂将是一个具有潜力的突破口。
科研助力当下,Disulfidptosis(双硫死亡)相关研究依旧如火如荼,TargetMol® GLUT 抑制剂 可助力您靶向 Disulfidptosis 后续的药物研发。如感兴趣或有疑问可私聊 T 仔咨询噢~ 关注公众号:陶术生物即时获取最新鲜的全球科技资讯! 参考资料: [1] Liu X, Olszewski K, Zhang Y, et al. Cystine transporter regulation of pentose phosphate pathway dependency and disulfide stress exposes a targetable metabolic vulnerability in cancer. Nat Cell Biol. 2020;22(4):476-486. doi:10.1038/s41556-020-0496-x [2] Liu X, Nie L, Zhang Y, et al. Actin cytoskeleton vulnerability to disulfide stress mediates disulfidptosis [published online ahead of print, 2023 Feb 6]. Nat Cell Biol. 2023;10.1038/s41556-023-01091-2. doi:10.1038/s41556-023-01091-2
|  |手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033
|手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033