2022年上半年29个新药获批,下半年有望获批的重磅首仿品种预测
近年来,国家层面鼓励首仿药,研发水平较高的头部药企在积极布局创新药的同时,也加快推进“抢仿”工作;首仿获批品种数逐年创新高,从2019年的53个,到2021年的78个,至2022H1已达到40个。
据相关媒体统计,在刚刚结束的上半年,国家药监局共批准了29款新药,包括18款化学药品、10款生物制品(涵盖单抗、疫苗)和1款中药。其中有18款新药是通过优先审评程序加速获批,占比62.1%。
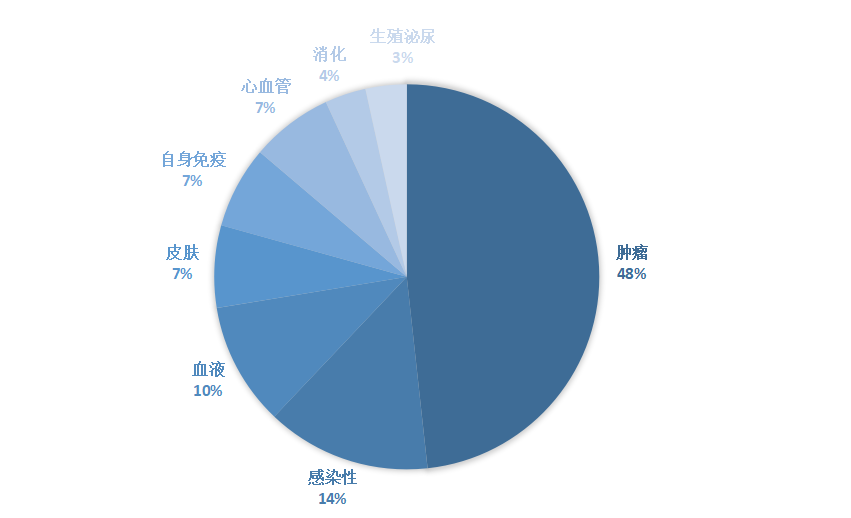
多款抗肿瘤新药获批,创“首个”记录
根据行业媒体的数据统计,今年上半年共有14款抗肿瘤新药获批。从适应症上来看,既有非小细胞肺癌、乳腺癌、胃癌、前列腺癌等细分癌种,也有高度微卫星不稳定型(MSI-H)实体瘤及NTRK基因融合肿瘤等泛瘤种适应症。这其中不乏多款药物在同靶点领域创下了“首个”获批的记录,为患者带来了全新的治疗选择。
01 基石药业引进的艾伏尼布片获批治疗携带IDH1易感突变的成人复发或难治性急性髓系白血病(AML),成为了首个在中国获批的IDH1抑制剂; 02 石药集团引进的度维利塞胶囊获批治疗复发或难治性滤泡性淋巴瘤成年患者,这是首个在中国获批的PI3K选择性抑制剂; 03 信达生物引进的佩米替尼片获批治疗FGFR2融合或重排的特定胆管癌成人患者,该药也是首个在中国获批的选择性FGFR受体酪氨酸激酶抑制剂; 04 云顶新耀引进的戈沙妥珠单抗获批用于转移性三阴性乳腺癌的二线治疗,这是首个在中国获批的靶向TROP-2的ADC,也是云顶新耀公司首款获批上市的新药; 05 拜耳公司的硫酸拉罗替尼胶囊获批治疗携带NTRK融合基因的实体瘤成人和儿童患者,该药是全球首款专为NTRK基因融合癌症患者设计的口服TRK抑制剂,也是首款在中国获批的TRK抑制剂; 06 康方生物的卡度尼利单抗获批治疗复发或转移性宫颈癌,这不仅是全球首个获批的PD-1/CTLA-4双抗,也是首款获批的由中国公司开发的双特异性抗体。
除了上述药物,诸多肿瘤适应症还迎来了创新疗法。在实体瘤领域,来自远大、礼来、辉瑞、恒瑞医药、复宏汉霖、武田(Takeda)、施维雅(SERVIER)等公司的药物,为结直肠癌肝转移灶、晚期胃癌、非小细胞肺癌、高瘤负荷的转移性激素敏感性前列腺癌、不可切除或转移性MSI-H成人晚期实体瘤、转移性胰腺癌等患者提供了新选择。
其中,远大医药的放射性药物SIR-Spheres 钇[90Y]微球注射液是中国首个获得批准用于治疗结直肠癌肝转移灶的产品,礼来公司的雷莫西尤单抗是中国首个被批准用于晚期胃癌二线治疗的靶向药物。

图片源于网络
在血液癌症领域,李氏大药厂引进的烷化剂药物盐酸丙卡巴肼胶囊、石药集团的盐酸米托蒽醌脂质体注射液等,分别为晚期霍奇金淋巴瘤、外周T细胞淋巴瘤等患者带来了新选择。
罕见病、儿童患者等迎来新药
近年来,罕见病、儿药受到国家的重点关切,自上而下出台一系列关于支持和鼓励罕见病和儿药开发的相关政策,受此影响,在今年上半年,亦有多款罕见病、儿童药物获批,给患者带来了新的治疗选择。
罕见病领域,苏庇医药申请的依马利尤单抗注射液通过优先审评程序于今年3月获批,用于特定的原发性噬血细胞性淋巴组织细胞增多症(HLH)成人和儿童患者的治疗。公开资料显示,依马利尤单抗于2018年在美国获批,是FDA批准的首款针对HLH的抗体疗法,代表着治疗原发性HLH领域20多年来的首个重大突破。
国家药监局官网截图
翰森制药引进的伊奈利珠单抗也于今年3月获批,用于治疗抗水通道蛋白4(AQP4)抗体阳性的视神经脊髓炎谱系疾病(NMOSD)成人患者。作为一款抗CD19单抗,伊奈利珠单抗可通过靶向CD19+B细胞,更广泛更持久地耗竭B细胞,持续降低NMOSD复发。翰森制药曾在新闻稿中表示,伊奈利珠单抗的获批标志着中国NMOSD治疗进入新纪元。
李氏大药厂引进的利鲁唑口服混悬液也于今年6月获批,为肌萎缩侧索硬化(ALS,又称“渐冻人症”)患者带来了新的治疗选择。(内容来源:博济医药股份)
与此同时,儿科疾病领域也迎来一些新药。例如,李氏大药厂引进的血管扩张剂吸入用一氧化氮获批,用于治疗患有低氧性呼吸衰竭并伴随肺动脉高压的足月及早产新生儿。
骄阳夏日,7月如期而至,2022年上半年的成绩单已尘埃落定,展望下半年,看看哪些重磅首仿药能获批上市?
2022下半年有望获批的重磅首仿品种
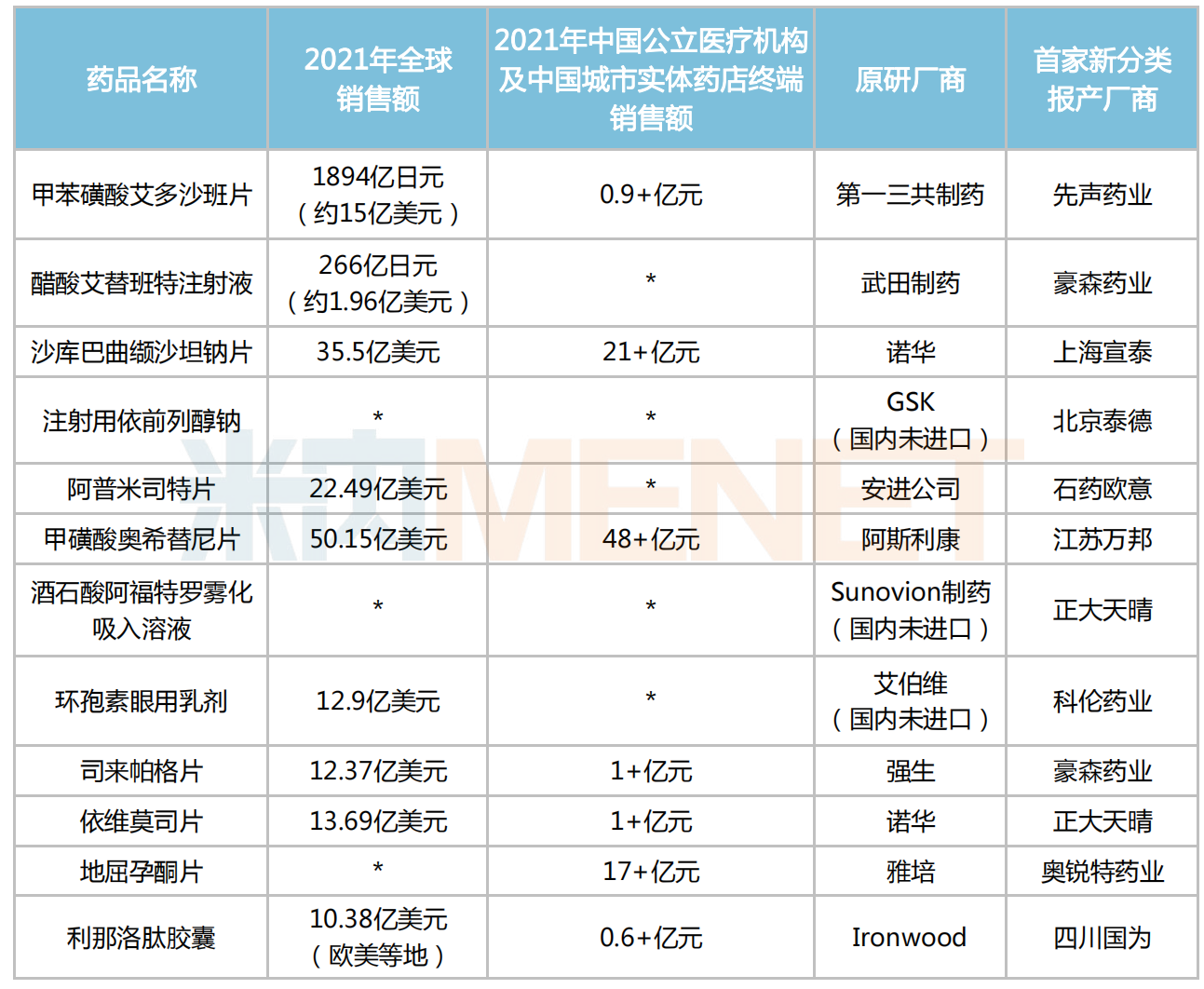
*声明:本文内容转载于网络,版权归原作者所有,转载目的在于传递信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除!
(https://mp.weixin.qq.com/s/Zyn3zLLqkWpipq1VAkM7kQ)



