曾因未遵守GMP规范,涉及生产记录真实性等,某药企被停产停业!
9月5日,辽宁省药监局发布1则行政处罚通知。辽宁可济药业有限公司未遵守药品生产质量管理规范,处125万元罚款,责令停产停业整顿1个月
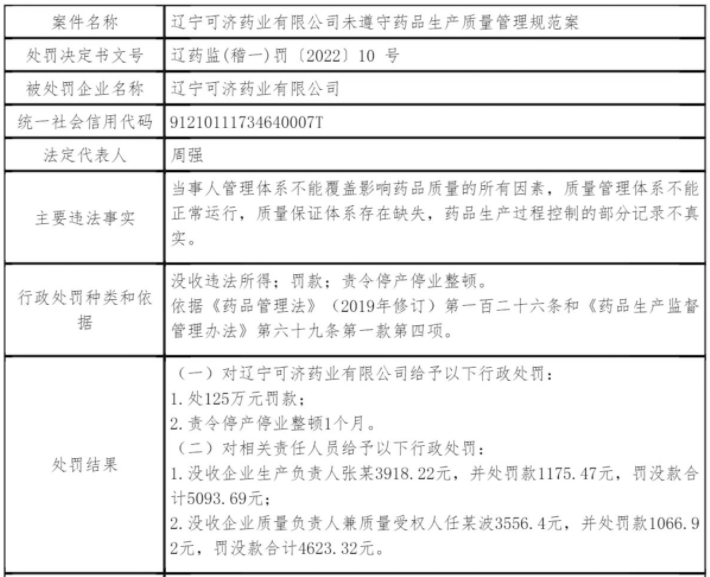
①辽宁可济药业有限公司未遵守药品生产质量管理规范案
主要违法事实
当事人管理体系不能覆盖影响药品质量的所有因素,质量管理体系不能正常运行,质量保证体系存在缺失,药品生产过程控制的部分记录不真实。
行政处罚种类和依据
没收违法所得;罚款;责令停产停业整顿
依据《药品管理法》(2019年修订)第一百二十六条和《药品生产监督管理办法》第六十九条第一款第四项
《药品管理法》(2019年修订)
第一百二十六条 除本法另有规定的情形外,药品上市许可持有人、药品生产企业、药品经营企业、药物非临床安全性评价研究机构、药物临床试验机构等未遵守药品生产质量管理规范、药品经营质量管理规范、药物非临床研究质量管理规范、药物临床试验质量管理规范等的,责令限期改正,给予警告;逾期不改正的,处十万元以上五十万元以下的罚款;情节严重的,处五十万元以上二百万元以下的罚款,责令停产停业整顿直至吊销药品批准证明文件、药品生产许可证、药品经营许可证等,药物非临床安全性评价研究机构、药物临床试验机构等五年内不得开展药物非临床安全性评价研究、药物临床试验,对法定代表人、主要负责人、直接负责的主管人员和其他责任人员,没收违法行为发生期间自本单位所获收入,并处所获收入百分之十以上百分之五十以下的罚款,十年直至终身禁止从事药品生产经营等活动。
《药品生产监督管理办法》
第六十九条 药品上市许可持有人和药品生产企业未按照药品生产质量管理规范的要求生产,有下列情形之一,属于《药品管理法》第一百二十六条规定的情节严重情形的,依法予以处罚:
(一)未配备专门质量负责人独立负责药品质量管理、监督质量管理规范执行;
(二)药品上市许可持有人未配备专门质量受权人履行药品上市放行责任;
(三)药品生产企业未配备专门质量受权人履行药品出厂放行责任;
(四)质量管理体系不能正常运行,药品生产过程控制、质量控制的记录和数据不真实;
(五)对已识别的风险未及时采取有效的风险控制措施,无法保证产品质量;
(六)其他严重违反药品生产质量管理规范的情形。
处罚结果
(一)对辽宁可济药业有限公司给予以下行政处罚
1.处125万元罚款;
2.责令停产停业整顿1个月
(二)对相关责任人员给予以下行政处罚
1,没收企业生产负责人张某3918.22元,并处罚款1175.47元,罚没款合计5093.69元;
2,没收企业质量负责人兼质量受权人任某波3556.4元,并处罚款1066.92元,罚没款合计4623.32元。

9月5日,江苏省药监局发布1则行政处罚通知。徐州辉眸医疗科技有限公司在未经许可的生产场地生产第二类医疗器械,被罚110万元!
②徐州辉眸医疗科技有限公司
违法行为类型
《医疗器械生产监督管理办法》(2017年修订)第四十五条的规定、第四十条
违法事实
徐州辉眸医疗科技有限公司在未经许可的生产场地生产第二类医疗器械等行为违反了《医疗器械生产监督管理办法》(2017年修订)第四十五条的规定、第四十条的规定,依据《医疗器械生产监督管理办法》(2017年修订)第六十一条第(四)项、第六十九条第一款第(一)项、《医疗器械监督管理条例》(2017年修订)第六十三条第一款第(二)项的规定,应予处罚。
处罚依据
《医疗器械生产监督管理办法》(2017年修订)第六十一条第(四)项、第六十九条第一款第(一)项、《医疗器械监督管理条例》(2017年修订)第六十三条第一款第(二)项
处罚类别
警告;罚款;没收违法所得、没收非法财物
处罚内容
1、警告;
2、没收免散瞳眼底照相机20台(编号FC21A001-020);
3、罚款110万元。
罚款金额(万元)
110

来源:网络整理,文章、图片等所有内容,仅用于学习交流,若有侵权内容及其他涉法内容,请及时联系删除或修改,特此声明!
*声明:本文内容转载于网络,版权归原作者所有,转载目的在于传递信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除!
(https://mp.weixin.qq.com/s/3YZzSfWoFZ-pweFf_XP1kg)



