全球上市仅3个月,被列参比?!
国内参比制剂目录已经遴选超100批,能被纳入的品种越来越少。2026年2月25日公布的第104批参比制剂征求意见稿中,新增品种仅10个,其中有两个均来自赛诺菲的新药。
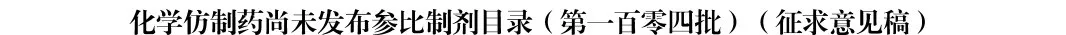
这款药全球上市时间很短,最早于2025年3月28日在美国获批(商品名Qfitlia),距今还不到一年时间。
血友病虽然属于罕见病,但患者规模并不算小。全球已登记患者超过87万人。目前临床仍以凝血因子替代治疗为主,但此类疗法半衰期较短、给药频繁,因此新机制疗法成为研发重点。
当前血友病领域最具代表性的药物之一,是罗氏的艾美赛珠单抗。
这是一款20多年来首个全新机制的非凝血因子替代治疗药物,2017年在美国率先上市后迅速放量。根据罗氏2025年财报,Hemlibra全年销售额达到47.54亿瑞士法郎,同比增长11%,目前仍是全球销售额最高的双抗药物。
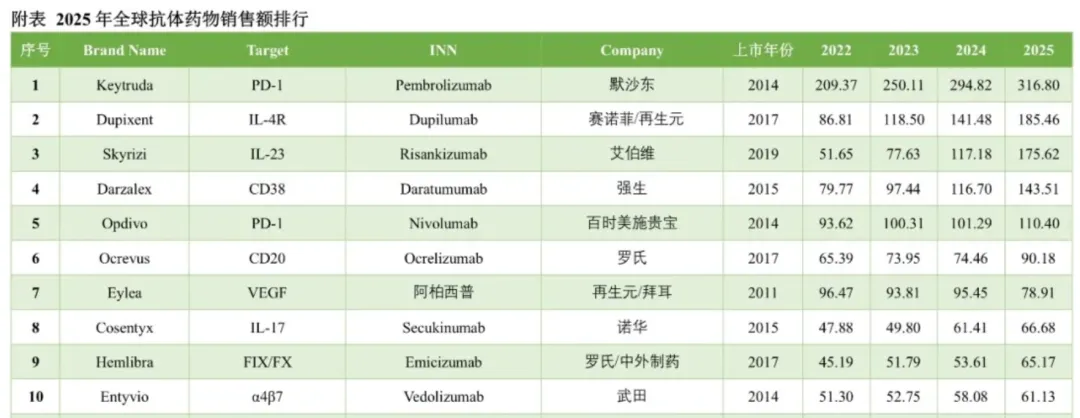
图源:中国医药创新促进会
芬妥司兰钠某种程度上正是瞄准这一市场。作为另一种具有开创性的siRNA疗法,它开创了每年仅需6次皮下注射的治疗模式,在给药频率上较Hemlibra进一步降低。
目前血友病领域竞争愈发激烈,除了罗氏Hemlibra,还有诺和诺德Alhemo和辉瑞Hympavzi 等新疗法也已陆续上市,不过凭借更广泛的适用人群与便捷给药方案,Qfitlia仍被业内寄予厚望。
再看第二款新药,阿夫凯泰片。
阿夫凯泰是目前肥厚型心肌病领域被认为具有“同类最佳”潜力的治疗药物,由Cytokinetics自主研发。
2020年7月,Cytokinetics与箕星药业达成合作,将阿夫凯泰片的大中华区独家开发与商业化权益授权给箕星,2024年,该权益又被转售给赛诺菲。
这款药物的上市时间更短。阿夫凯泰片首先在中国获批,时间为2025年12月16日,商品名“星舒平”;三天后才在美国获批。换言之,该药全球上市至今也仅约三个月。
该品种在国内的上市许可持有人为Cytokinetics公司,赛诺菲负责商业化推广,专利2039年1月才到期。
从机制上看,阿夫凯泰属于第二代心肌肌球蛋白抑制剂。肥厚型心肌病在我国发病率同样不低,根据国内普通人群抽样调查,成人患病率约为1/625,约每200人中就有1人患病。
目前这一赛道的首款药物是第一代心肌肌球蛋白抑制剂,来自BMS公司旗下的玛伐凯泰。该药于2022年在美国上市,2024年进入中国市场。根据BMS年报数据,玛伐凯泰2024年全球销售额已达到6亿美元。
在国内市场,该药2025年被纳入医保后增长迅速,仅前三季度销售额便已突破亿元规模。
虽然玛伐凯泰与阿夫凯泰同属心肌肌球蛋白抑制剂,但二者在分子机制及适用人群上存在差异。等到阿夫凯泰进入医保,其国内市场表现同样不可小觑。
整体来看,这两款新药都属于最新一代治疗技术,在各自领域均被业内寄予较高预期。但由于上市时间极短,市场空间仍有待验证,同时专利保护期仍然很长。
在这种背景下,国内企业已经开始提前布局参比制剂,节奏明显比以往更早。
*声明:本文内容转载于网络,版权归原作者所有,转载目的在于传递信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除!
(https://mp.weixin.qq.com/s/SZR_5hNmN3ClpP_umnzcHA)



