心源性猝死,药物如何介入管理
相关数据显示,我国每年约有55万人发生心源性猝死,急救黄金时间只有4-6分钟,而救护车平均到达时间通常在8-13分钟,院前往往存在明显的“急救空窗期”。也正因为这种强烈的突发性和高致死性,张雪峰去世后,大家都很关心:有没有药,可以提前阻止SCD。
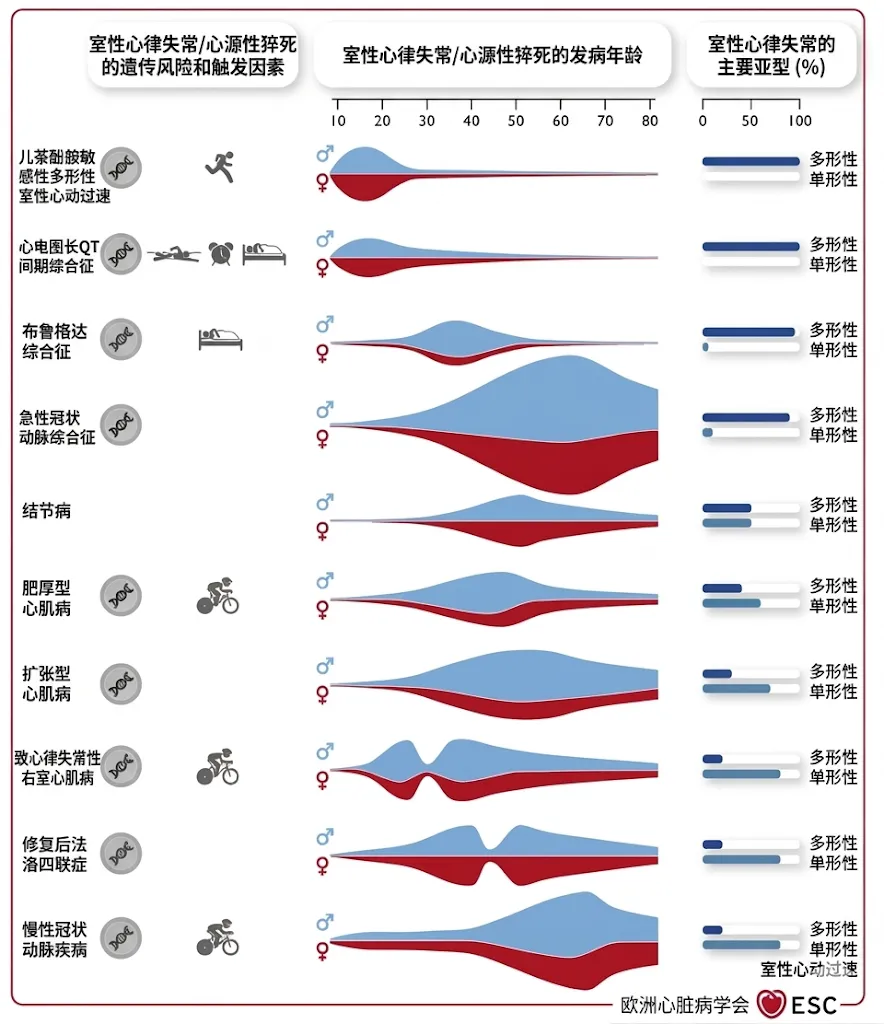
SCD不是一个单独疾病,而是多种基础心脏病在终末阶段的共同结局。心肌梗死后瘢痕、射血分数降低型心衰、肥厚型或扩张型心肌病、遗传性通道病,最后都可能表现为恶性室性心律失常和猝死(图1)。也正因为如此,药物对SCD的介入,并不是依赖某一个统一的“防猝死药”,而是分散在基础病治疗、特定高危场景下的抗心律失常管理,以及药物安全性控制等几个层面。
图1.不同疾病中室性心律失常/SCD的遗传风险、诱因、发病年龄、性别优势及心律失常类型
01
基础病治疗
01
基础病治疗
在SCD风险管理里,最容易被低估是基础病治疗药物。
对心肌梗死后和射血分数降低型心力衰竭患者来说,猝死风险升高往往不是某一次随机电活动异常,而是长期缺血、心室重构、纤维化和泵功能恶化等多种高风险因素异常共同把心脏推向了更不稳定的状态。在这样的病程里,能改变风险的并不是单次抢救,而是更早期的药物干预。
其中,β受体阻滞剂是最典型的一类。它们通过抑制交感神经过度激活,减少儿茶酚胺驱动的室性心律失常触发,同时降低心肌耗氧量、减轻心脏负荷。对心肌梗死后和射血分数降低型心力衰竭人群表现出明显的症状改善,能够有效预防致命性室性心律失常和猝死风险。因此,酒石酸美托洛尔、富马酸比索洛尔、卡维地洛这类药物长期占据高危人群治疗底盘,因为它们在更长时间尺度上改变了风险背景。
此外,对高危心肌来说,猝死很多时候不是一个单纯的节律问题,而是结构异常、传导异常和神经激素失衡累积到一定程度后的最终表现。血管紧张素转换酶抑制剂和血管紧张素Ⅱ受体阻滞剂通过抑制肾素-血管紧张素-醛固酮系统减缓这一进程,血管紧张素受体脑啡肽酶抑制剂则在此基础上进一步改善心力衰竭病程。AHA/ACC/HFSA 2022心力衰竭指南把这几类药物放在射血分数降低型心力衰竭核心位置(图2)。
图2.AHA/ACC/HFSA 2022心力衰竭指南

图片来源:Circulation
盐皮质激素受体拮抗剂同样如此。螺内酯、依普利酮既能利尿或改善短期临床状态,还能够抑制纤维化和结构性恶化。从而降低心脏走向电不稳定、室性心动过速和室颤的概率。
因此,很多真正带有抗猝死价值的药物,通常是以心力衰竭药、抗重构药和长期慢病管理药的身份进入市场。从临床终点看,这些药物不只能够改善症状和减少住院,它们同时也在减缓患者进入恶性室性心律失常高风险区间的速度。
02
高危人群用药
02
高危人群用药
基础病治疗解决的是高危人群的底层风险,药物介入SCD的另一层面还体现在高危场景里。
胺碘酮、索他洛尔、氟卡尼、奎尼丁这类药物都与致命性心律失常等高危风险疾病相关,但适用场景、人群边界和临床目的差别很大。
其中,胺碘酮在室性心律失常控制、电风暴处理以及部分合并心力衰竭患者的节律管理中有明确效果。它可以减少室性心动过速和室颤负担,降低急性事件频率,在部分患者中也能减少植入式心律转复除颤器放电次数。因此,胺碘酮可用于特定场景下的室性心律失常控制和电风暴管理,而不是面向所有高危患者。
索他洛尔也类似。它兼具β受体阻滞和Ⅲ类抗心律失常作用,可用于部分室性心律失常患者,但其使用建立在对具体人群和具体风险平衡的判断之上,并不具备普适性。
相比之下,遗传性心律失常场景下的个体化用药,边界更清楚。氟卡尼主要用于儿茶酚胺敏感性多形性室性心动过速。这类患者在儿茶酚胺刺激下极易触发致命性室性心律失常。奎尼丁则更多见于Brugada综合征、短QT综合征或室颤电风暴等更窄的人群。
至于硝酸甘油、硝酸异山梨酯这类硝酸酯药物,其作用更多体现在改善缺血背景、缓解冠脉痉挛和症状负担,从而减少部分患者被进一步推入危险状态的概率。它们同样有明确的适用人群,但并不是SCD预防中的核心用药。
03
安全性边界
药物与SCD关系最紧的一端,其实在安全性。药源性QT间期延长是一种心电生理异常,若延长显著,可能导致尖端扭转型室性心动过速,进而发展为室颤、猝死,是最典型的致命性心律失常问题之一。对很多企业来说,如何避免药物把患者推向更高的致命性心律失常风险,是一条非常现实的研发和商业边界。
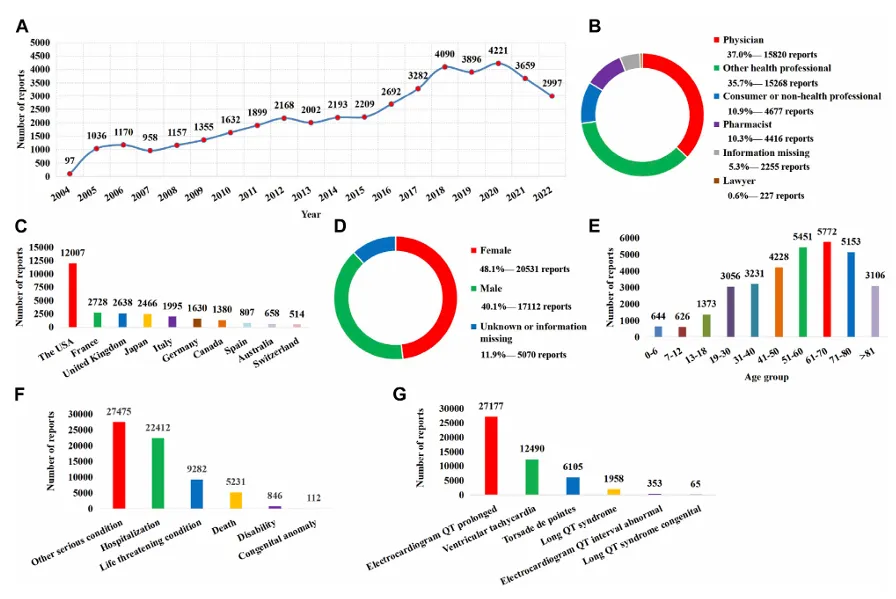
2023年一项基于FAERS数据库的研究显示,2004年至2022年间,与QT间期延长和尖端扭转型室性心动过速相关的不良事件报告达到42713份,涉及1088种潜在相关药物,且抗肿瘤药占比最高(图3)。这意味着,药源性致命性心律失常风险并非少数心血管药物的局部问题,而是多个治疗领域的真实安全性边界。
图3.与QT延长和尖端扭转相关的报告的基本信息和临床特征
图片来源:Frontiers
对药企而言,安全性决定了一款药物能否进入市场,也决定了其能否在真实世界中稳定使用。很多企业并没有开发所谓“防猝死药”,却始终投入大量资源确保自己的产品不要制造新的致命性心律失常风险。
然而,风险很少由某一个分子单独造成。更常见的是多重因素叠加,药物联用、代谢酶抑制、肝肾功能异常、电解质紊乱以及患者自身的基础易感性,往往共同决定了风险是否真正暴露。对企业来说,真正的挑战是把这些风险边界定义清楚,并进一步把安全性转化为真实的临床和商业竞争力。
对医药行业来说,更值得关注的是,药物究竟通过什么方式介入SCD的风险管理。
在这里,我们认为基础病治疗在压低长期风险,特定场景下的抗心律失常药在管理高危事件,安全性体系则在守住最后一道风险边界。SCD是心力衰竭药、精准心律失常项目和安全性平台共同面对的综合命题。
*声明:本文内容转载于网络,版权归原作者所有,转载目的在于传递信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除!
(https://mp.weixin.qq.com/s/F9aiaDl4YFQ9gK-37qIQyA)



